서 론
지질 및 폐탄광 현황
연구방법
시료채취 및 분석방법
현장수질 측정 및 성분분석
포화지수 및 화학종 계산
결과 및 고찰
AMD의 수질특성과 이온함량
AMD의 포화지수와 화학종 분포
AMD 침전물의 광물종 분석: X-선 회절분석(XRD) 및 적외선 분광분석 결과
침전물의 초미세 구조적, 화학적 특징: 주사전자현미경 분석결과
배스알루미나이트질 침전물의 나노결정구조(nanocrystalline structure) 특징: 핵자기공명(27Al NMR)분석결과
알루미늄의 발생과 제어
결 론
서 론
폐탄광(abandoned coal mine)으로부터 발생하는 산성광산배수(acid mine drainage, AMD)인 오염 유출수는 수생태계와 수질에 악영향을 끼칠 수 있으며, 게다가 산성으로 인해 교량이나 하천에 설치된 구조물의 초기 설계시의 예상수명을 단축시키거나, 심각한 손상을 줄 수 있다. AMD의 주요 성분인 철, 황, 알루미늄은 용존되어 이동하거나, 적절한 pH, Eh, 용해도 조건하에서 화학적, 미생물학적(microbial) 작용에 의하여 하상에 침전된다. 이 과정에서 철, 알루미늄, 황산이온은 비소(As), 구리(Cu), 카드뮴(Cd) 등과 같은 유해원소와 공침(coprecipitation)하거나, 흡착되면서 수계의 환경을 제어하게 된다(Carlson et al., 2002). 따라서 AMD 수계를 따라 특정 성분이 용존상태로 이동하거나, 고상으로 침전되는 현상의 이해는 환경적인 대책방안을 수립하는 데 있어서 중요하다(Foos, 1997). 폐탄광의 AMD에서는 흔히 하상에 다양한 침전물이 피복되어 있으며, 이들은 다양한 Fe, Al 화합물로 구성된다(Kim et al., 2002,Kim et al., 2003; Woo et al., 2016; Lim et al., 2019). 대표적인 수산화철 및 수산화황산염 광물은 철과 황산이온의 함량이 높고, pH가 낮은 대부분의 AMD의 침전물에서 풍부하다(Rose and Elliott, 2000; Lee et al., 2002). 특히 결정도가 매우 낮은 광물인 슈베르트마나이트(schwertmannite)는 황산이온이 풍부한 광산수로부터 침전되는 대표적인 광물이다(Bigham et al., 1990, Bigham et al., 1996; Bigham and Nordstrom, 2000; Yu et al., 1999; Choo and Lee, 2002; Kim et al., 2002, Kim et al., 2003; Choo et al., 2004, Choo et al., 2007, Choo et al., 2008; Lee and Kim, 2008).
국내의 AMD 연구에서는 황철석(FeS2)의 산화작용의 결과물인 철의 역할과 기여도에 집중되어 온 경향이 있었다. 즉 황철석과 같은 황화물의 산화작용 동안 용탈되는 철 외에도 황화물의 상당 부분을 차지하는 황의 특성이 매우 중요함에도 불구하고, 이를 간과한 측면이 있다. 또한, 폐탄광의 모암에서는 석탄을 포함하여 상당량의 Al, Si 광물이 포함되어 있기 때문에 이런 AMD에서 유독성인 Al의 분산과 침전이 발생하는 원리와 메커니즘 이해는 여전히 부족하다.
지난 20여 년간 국내의 많은 폐광산 일대의 수계를 대상으로 AMD 발생을 억제하거나, 오염처리를 위한 처리시설이 전국적으로 건설되었으며, 그 결과 현재 어느 수준까지는 수계와 토양오염을 방지하는 효과를 보여 주는 것으로 평가된다. 그러나 산성광산 배수의 폐수처리시설 건설이후 부실한 사후관리와 제한적인 수명으로 인하여 현실적으로는 수계오염방지 성능이 제대로 작동하지 않는 곳도 여전히 존재한다. 그 동안 광해방지공단을 중심으로 국가적 차원에서 AMD 관리를 진행해 왔으나, 예산 및 접근성의 한계점으로 인하여 소규모의 폐광산의 경우 현재에도 오염방지시설 자체가 없거나, 방치된 곳이 다수 분포한다.
본 연구에서는 충청북도 단양군 대강면 ‧ 가곡면의 일대에 걸쳐 있었던 단양탄전에 속하는 봉양폐탄광을 대상으로 이 일대의 AMD의 오염현황과 수계의 침전물의 특성분석을 수행하였다. 이를 통하여 연구지역과 가까이에 위치하고 있는 월악산국립공원 구역과 충주댐으로 유입되는 큰 하천인 단양천의 수질오염 가능성과 관리대책 수립에 기본적인 정보를 제공할 수 있을 것으로 기대된다.
봉양폐탄광이 소재하는 곳은 월악산국립공원 영역에 포함되며, 봉양폐탄광은 지리적으로 열악한 여건 등으로 인해 지금까지 방치되어 있는 실정이다. 현재에도 회산천이 소재하는 연구지역의 AMD에서는 하상전체가 백색 내지 회백색의 침전물로 피복되어 있어서 하천의 경관에 심각한 영향을 줄 뿐만 아니라, 하천생태계는 물론 농작물에도 직간접적인 영향을 미칠 것으로 예상된다.
지질 및 폐탄광 현황
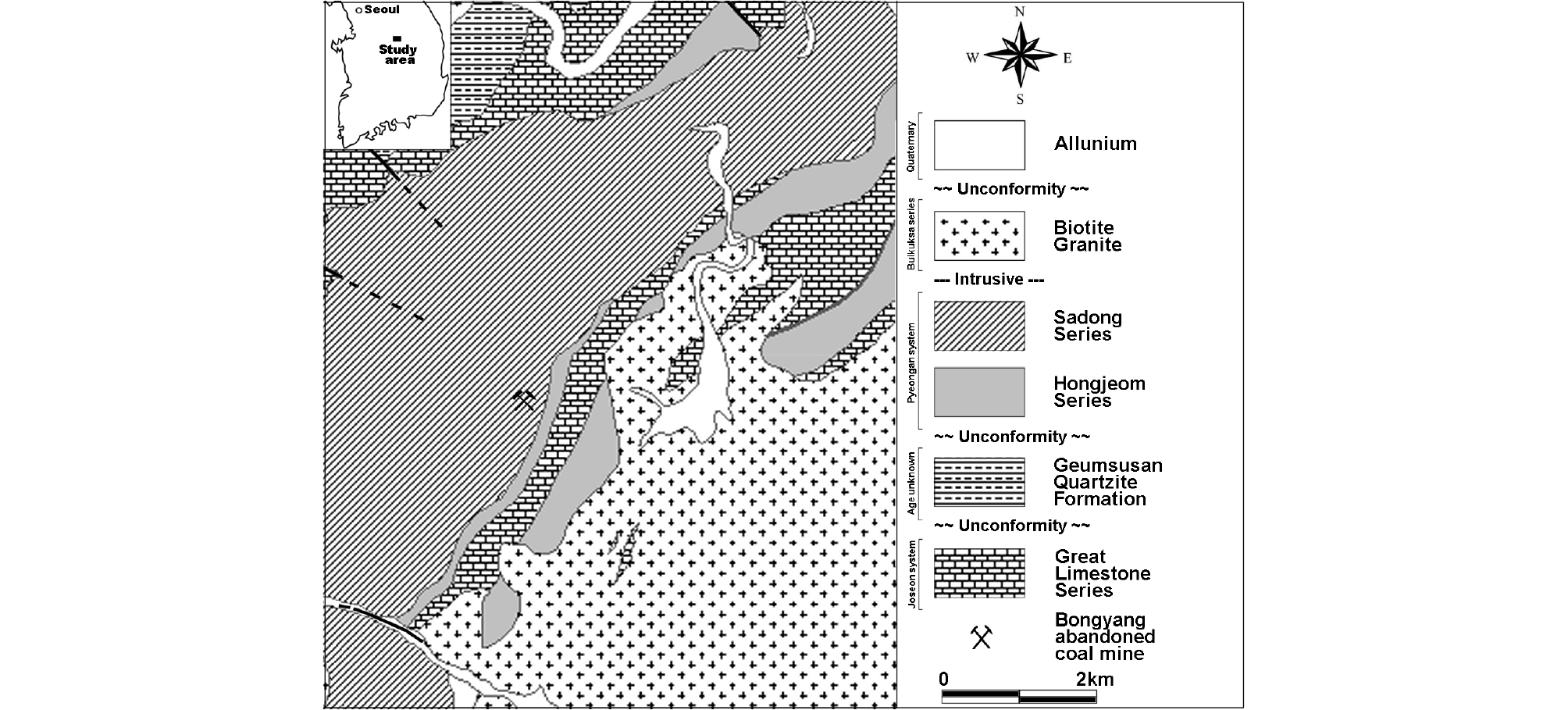
봉양폐탄광지역은 조선계 대석회암통을 기저로 평안계의 문수봉층, 사동통, 기촌층과 봉양층(고방산통)이 대상으로 분포하며, 용두산을 중심으로 중생대의 사평리역암층이 부정합으로 피복하며, 이들을 후기의 백악기 화강암이 관입 발달한다(Fig. 1). 이들 퇴적암류는 화강암의 관입으로 심하게 변질되어 있다.
대석회암통은 본 역 변성퇴적암층의 기저를 이루며 주로 회색 내지 담청색의 석회암으로 구성된다. 문수봉층은 홍점통에 대비되며, 사암층 내에 원마도가 불량한 역을 함유하고 있는 것이 특징이다. 본 층은 백색 내지 녹회색 석회암층과 역질 규암, 혼펠스 등 다양한 암상이 발달하며, 층후는 100~200미터에 달한다.
봉양폐탄광지역의 함탄층은 고생물학적 특징에 의해 평안계 사동통에 해당되는 것으로 알려져 있다. 탄광의 갱도를 중심으로 북부에는 하부셰일대, 중부규암대, 상부셰일대로 구성되며, 층후는 북부에서 최대 250미터에 달하지만 남부에서는 약 100미터로 얇아진다. 하부 셰일대는 2~3매의 불연속적인 탄층이 협재하며, 주로 흑색 세립질 규질사암과 흑색셰일로 구성된다. 중부 규암대는 유백색 규암으로 구성되며, 층후가 10~30미터로 비교적 얇고, 그 상위에 탄층이 발달한다. 상부 셰일대 내에는 연속성이 양호한 1매의 탄층이 협재하며, 흑색 세립질 규질사암, 흑색셰일 및 탄질셰일로 구성되고, 사동통의 표준화석인 인목(Lepidondendron)이 산출된다. 대한석탄공사 단양출장소가 대강면 ‧ 가곡면에서 무연탄을 1950년까지 채탄하였으나 그 뒤 휴업상태였으며, 1970년대에 이르러 중소탄광의 개발에 착수하여 현재 단양읍에 있는 단양탄광, 봉양탄광, 동화탄광을 비롯하여, 대강면 노동리의 동화탄광, 가곡면의 소백광업소 ‧ 보발광업소 및 대강면의 태일광업소 등에서 연간 약 200만∼250만톤이 생산되었다. 이 중에서 봉양탄광은 1960년대 후반에 연 10만톤 내외의 고품위 토상흑연을 생산한 바 있으며, 1980년대 초에는 연 15,000톤 내외, 1985년도에는 약 7,000톤 내외로 생산량이 급감하였다. 1989년 석탄산업 합리화정책으로 비경제적 탄광들이 정리되었고, 이에 근거하여 봉양탄광은 1990년에 폐광되었다.
봉양폐탄광은 해발 950미터 준봉의 북쪽 사면에 발달하는 계곡부에 존재하며, 해발 약 600미터에 소재한다. 이 일대는 계곡이 협소하고 경사가 급해 폐수처리 정화시설을 설치하기 쉽지 않은 것으로 보인다. 현재 봉양폐탄광은 운영 당시 채굴된 폐석이 북측 사면에 방치되어 있으며, 폐석에는 다량의 탄질셰일 및 저급 석탄이 다량 포함되어 있다. 또한 주갱은 개발 당시의 모습 그대로 방치되어 있으며, AMD가 지속적으로 배출되고 있다. 배출된 AMD는 계곡을 따라 복류하여 회산천에 합류 후, 회산리를 지나서 규모가 큰 단양천에 합류되는데, 이 단양천은 북향으로 흐른 후에 충주호로 유입된다.
연구방법
시료채취 및 분석방법
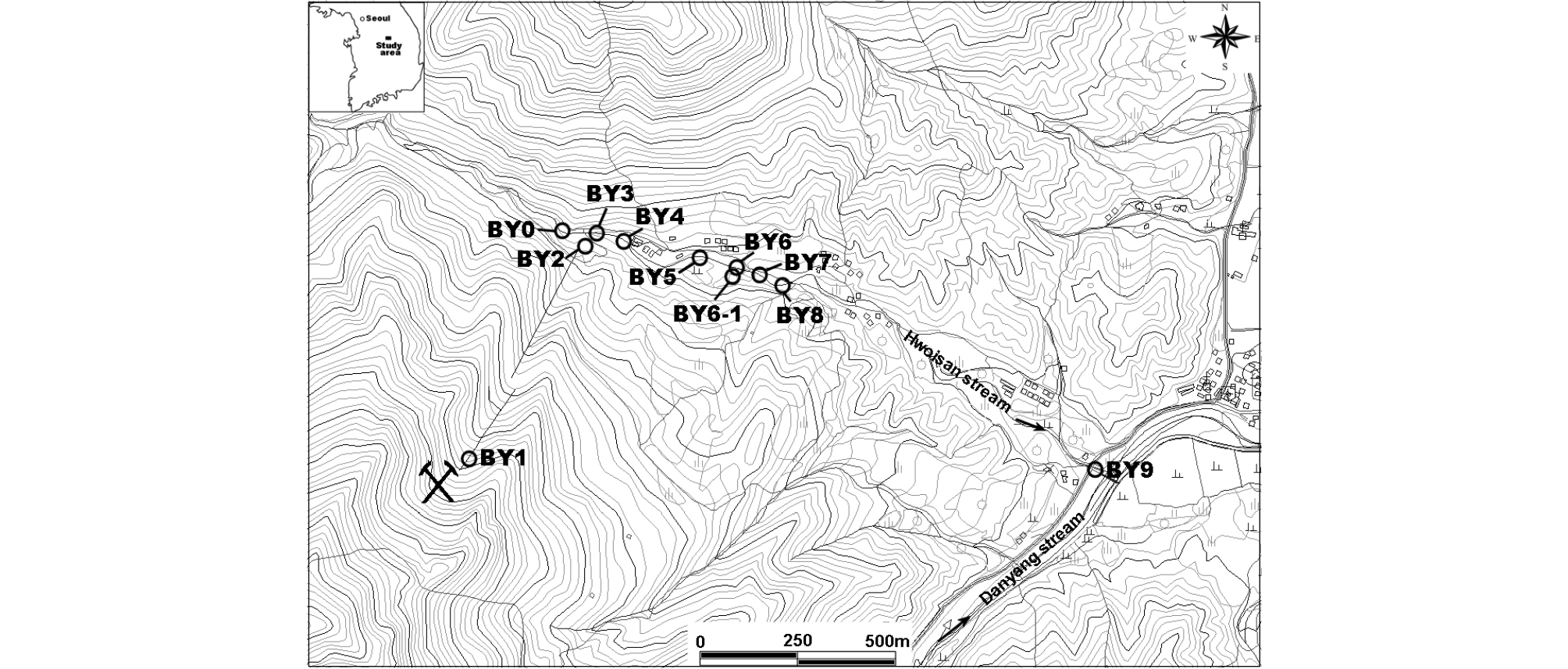
폐탄광의 영향이 없는 비오염지역 상류 하천수를 대조구(BY-0)로 설정하고 이를 하류천의 오염정도를 파악하는데 배경치로 활용하였다. 폐광산에서 유출된 AMD가 하천 생태계에 미치는 영향을 분석하기 위하여 하천수의 수질과 퇴적물을 채취하였다. 하천수와 퇴적물 분석을 위한 조사는 2016년 9월에 실시하였다. 조사 시 침출수, 침출수가 혼입된 회산천의 하천수, 침출수로부터 침전된 하상퇴적물 등을 대상으로 조사하였다. 조사지점의 특징은 다음과 같다(Fig. 2).
BY-0: 회산천 상류부 비오염하천수(대조구)
BY-1: 봉양폐탄광의 폐갱 유출수
BY-2: 폐광산 계곡 말단부 복류수(AMD)
BY-3: AMD의 일부가 본류에 유출되는 지점
BY-4: BY-2의 AMD 복류수가 회산천 본류에 혼입되는 지점
BY-5: 회산천 중류의 보
BY-6-1: AMD 저류지의 방류구
BY-6: AMD 저류지 방류수가 회산천 본류에 합류 후 지점
BY-7: 분홍색 하상 퇴적물이 출현하는 지점
BY-8: 회산리 마을 중간 지점
BY-9: 회산천의 최하류 지점(단양천 합류 전)
봉양폐탄광의 폐갱에서 직접 유출되는 AMD는 Yellow boy 현상이 심한데, 이로 인해 다량의 철수산화물 침전물이 하상에 존재한다(Figs. 3, 4). 폐갱구 입구의 AMD(BY-1)는 급경사의 하천을 따라 유동하며, 계곡부에 산재하는 폐석 등의 하부를 복류하면서 회산천에 합류된다. 합류지점에서 AMD는 하천바닥에서 샘처럼 복류하여 지하의 다양한 경로로 혼입되는 것이 관찰된다. 갱구입구 BY-1 지점 수계바닥에서 흔히 발견되는 침전물은 Munsell Rock-Color Chart에 의하면 짙은 노랑오렌지(dark yellowish orange)의 10YR 6/6 색상을 띤다. BY-3, BY-4 지점과 같이 회산천 본류에는 AMD가 합류되면서 회백색의 침전물이 생성되기 시작하는데, 회산리를 거쳐 최하류까지 이 같은 회백색 침전물이 다량 발달하고 있다.
현장수질 측정 및 성분분석
하천수는 현장에서 pH, Eh, EC 등을 측정하고, 0.45 µm PVDF 필터를 사용하여 여과 후, 채수하였으며, 양이온 분석용 시료는 현장에서 질산처리를 하였다. 경북대학교 공동실험실습관의 유도플라즈마분광분석기(ICP, ICAP-7600), 유도플라즈마질량분석기(ICP-MS, NexION)로 양이온을 분석하였으며, 음이온은 여과 후 진공튜브에 채수하여 이온크로마토그래피(IC, ICS-5000, Dionex)로 분석하였다.
하상퇴적물 채취 시에는 하상에 부착된 침전물을 일회용 스포이드를 사용하여 채취하였으며, 실험실 건조기를 이용하여 40℃ 하에서 24시간 이상 충분히 건조한 후에 하상 침전물을 구성하고 있는 광물의 미세조직, 결정형태, 입자관찰을 수행하였다. 한국기초과학지원연구원 대구센터에서 초고해상도 전계방출형 주사전자현미경(Ultra High Resolution Field Emission Scanning Electron Microscope, Hitachi S-4800 UHR FE-SEM), 전계방출형 주사전자현미경(Field Emission Scanning Electron Microscope, Hitachi S-4200 FE-SEM)을 이용하여 침전물의 초미세조직과 화학분석을 수행하였다. 시료는 오스뮴(OS)으로 코팅하였으며, 20 kV/10 nA 조건하에서 40~7만 배율로 관찰하였다. 화학분석은 주사전자현미경의 에너지분산 스펙트럼(energy-dispersive spectrum, EDS)을 이용한 미세결정 입자에 대한 화학분석을 실시하였다.
X-선 회절분석기(MF-XRD)를 이용하여 침전물의 광물종 파악과 결정도 분석을 수행하였으며, 5~65도 2θ 범위에서 Cu 타켓을 사용하였다. 침전물질의 분자결합특성 분석을 위하여 적외선분광분석(Fourie transform Infrared spectroscopy, PerkinElmer IR Frontier model)을 이용하여 650~4,000 cm-1 파수(wavenumber) 범위, 해상도는 0.4 cm-1로 측정하였다. 비정질 나노 알루미늄 침전물의 원자단위의 구조특성 분석을 위하여 경북대학교 공동실험실습관의 고체 핵자기공명분석기(Solid-state nuclear magnetic resonance spectroscopy, 400 MHz Bruker AVANCE III HD 400 model)를 사용하였다.
포화지수 및 화학종 계산
AMD 오염수에 존재할 수 있는 주요 광물의 포화지수(saturation index)와 대표적인 화학종(chemical species) 비를 계산하였다. 이를 위하여 US EPA의 MINTEQA2를 개량한 Visual MINTEQ v.3.1을 사용하였으며, pH, Eh 및 수질화학 조성치를 입력하였다.
결과 및 고찰
AMD의 수질특성과 이온함량
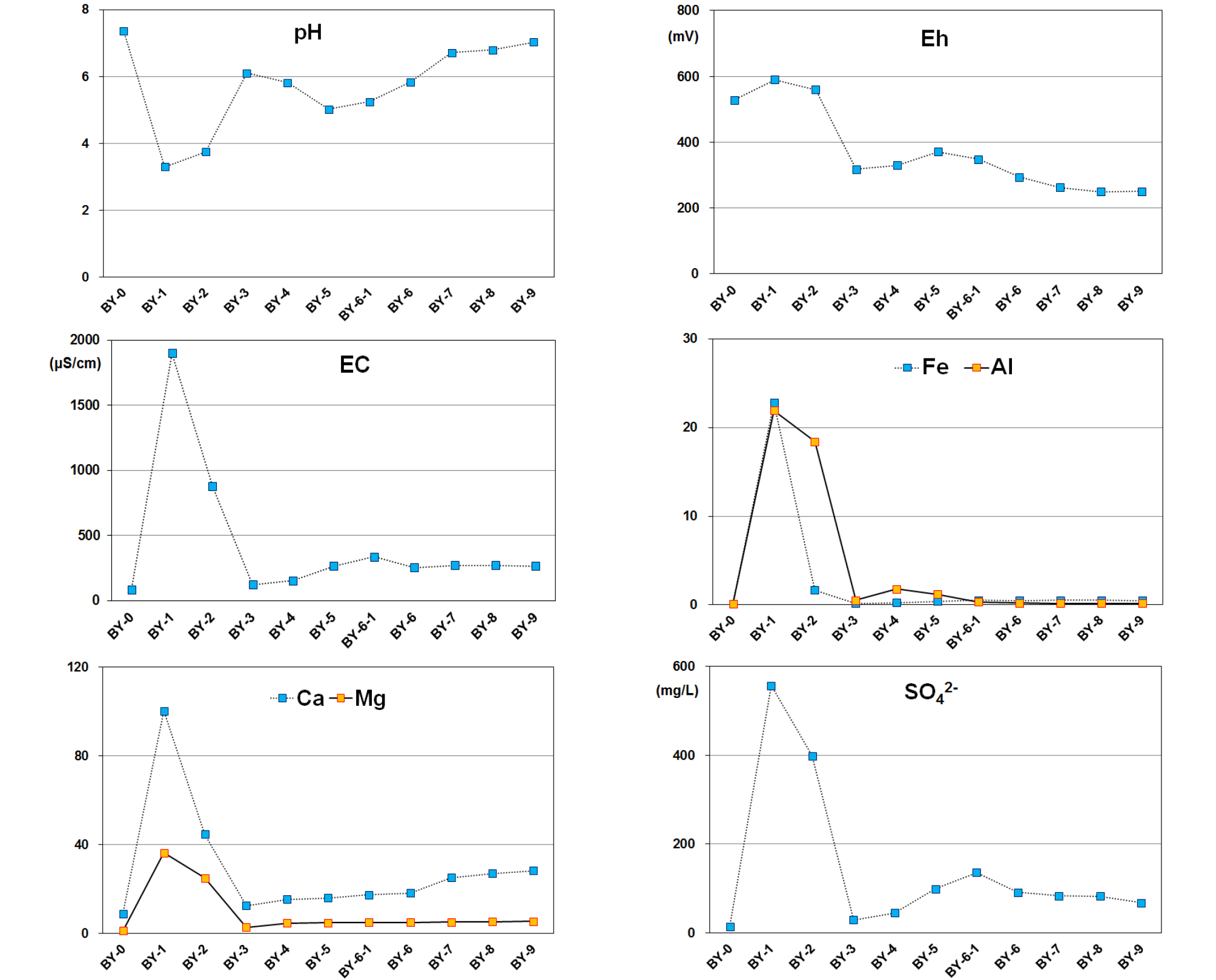
봉양폐탄광의 폐갱에서 유출되는 AMD는 pH가 3.3으로 산성이며, 회산천에 합류 후 하류로 갈수록 점증하여 하류부에서는 7.04로 중성을 보인다(Table 1, Fig. 5). 이러한 특징은 조사지역 비오염하천의 pH 7.36보다 공히 낮은 것이 특징이다. 폐갱 AMD(BY-1)와 복류구간 말단부의 침출수(BY-2)의 Eh는 각각 590 mV, 560 mV로 전형적인 AMD의 특징을 보이며, 회산천 합류후 하류로 갈수록 점점 감소하는 특징이 있다. 이는 회산천변에 산재하는 농경지, 농가 등으로부터 유입되는 유기물 등 다양한 오염물질의 영향으로 판단된다.
Table 1. Physicochemical properties of the Bongyang AMD. Chemical concentration unit is mg/L unless otherwise noted
대조구로 설정한 비오염 회산천도 철과 알루미늄의 함량이 각각 0.14 mg/L, 0.13 mg/L로서 비교적 높은 함량을 보이는 것은 회산천의 상류 유역에도 함탄층 등이 산재하기 때문으로 보인다. 봉양폐탄광의 폐갱의 AMD는 철과 알루미늄의 함량이 각각 22.82 mg/L, 21.94 mg/L로 현저히 높고, 회산천 합류 후에는 그 값이 현저히 감소하지만 하천의 전 구간에서 철은 0.5 mg/L 내외, 알루미늄은 0.18 mg/L 내외로 먹는물 기준을 현저히 상회하는 구간이 많다. 황산이온의 함량도 폐갱 AMD 및 복류구간 말단부 침출수에서는 각각 557 mg/L, 398 mg/L로 높지만 회산천에 합류 후에는 현저히 낮아진다. 이는 AMD로부터 침전된 침전물 중 슈베르트마나이트 등의 생성으로 제거되기도 하지만 비오염하천수의 혼입에 의한 희석 등의 영향이 큰 것으로 판단된다.
갱구 유출수(BY-1)는 강산성의 pH, 높은 Eh, EC를 보이며, 특히 Fe, Al, Ca, Mg, SO4의 함량도 가장 높다. 이들 용존 이온들의 농도는 회산천과 합류 후에는 희석작용으로 인하여 급격하게 감소하는데, 이 과정에서 용해도의 변화로 인하여 침전되면서 제거되는 효과도 예상된다.
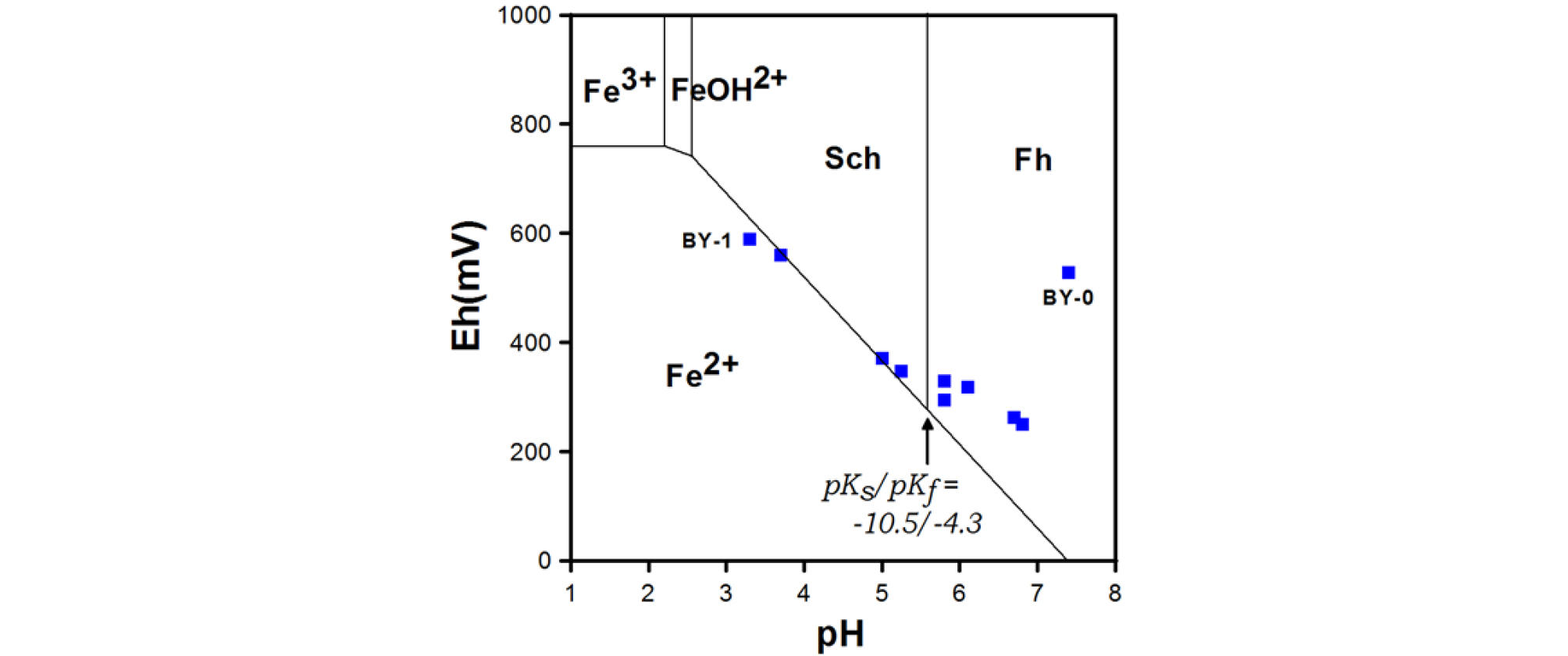
Fig. 6은 Eh-pH 다이아그램에 도시한 것으로서 철 이온이 다양하게 존재할 수 있음을 보여준다. AMD의 철 이온은 산화환원 상태와 pH에 따라서 화학종(chemical species)은 달라질 수 있는데, 갱구 유출수(BY-1)는 2가철의 상한 영역과 슈베르트마나이트 경계선 부근에 놓이나 여전히 2가철 상태이며, 대조구인 계곡수(BY-0)는 페리하이드라이트(ferrihydrite) 영역에 놓인다. 그 외 대부분의 시료들은 2가철과 슈베르트마나이트 경계선 부근에 도시된다.
AMD의 포화지수와 화학종 분포
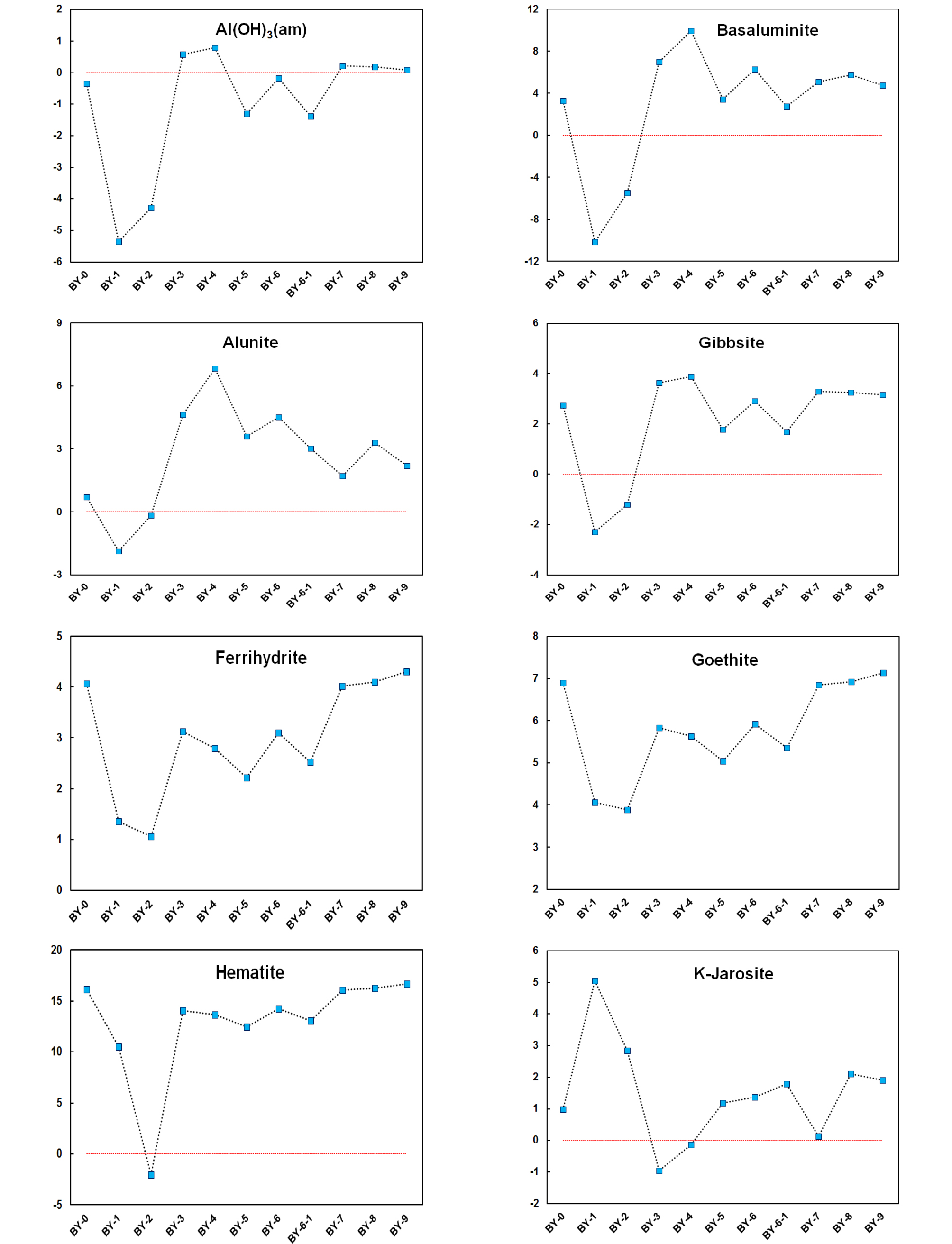
용존이온의 농도를 이용하여 포화지수(saturation index)와 화학종(chemical species)을 계산한 결과는 다양한 광물종이 용존이온의 지구화학적 조건에 따라서 존재함을 보여준다. 이는 용존이온의 실제 농도인 활동도(activity)를 주요 광물의 평형상수에 비교하여 이론적인 용해도를 파악하는 것으로, 수계 내에서 평형반응을 통하여 특정한 광물이 침전될 수 있음을 나타낸다(Table 2, Fig. 7).
Table 2. Saturation indices of Bongyang AMD water calculated by Visual MINTEQ. S.I.: saturation index
수산화알루미늄[Al(OH)3]은 갱구 유출수(BY-1)에는 불포화상태이며, 회산천과 합류되면서 포화상태에 도달한다. 그러나 중하류로 가면서 불규칙하게 포화, 불포화 상태를 보이다가 하류로 가면서 포화상태를 지속한다. 수산화황산알루미늄 광물인 배스알루미나이트(basaluminite: Al4(SO4)(OH)10 ‧ 4-5H2O)는 갱구 유출수와 그 직 하류(BY-2)를 제외하면, 회산천 일대를 거쳐 높은 과포화상태를 나타낸다. 대표적인 수산화황산알루미늄 광물인 명반석(alunite)과 수산화알루미늄 광물인 깁사이트(gibbsite)도 갱구 유출수의 성분에 영향을 강하게 받는 AMD 인 BY-1, BY-2 지점을 제외하면, 높은 과포화상태를 나타낸다. 이로 보아 알루미늄이 함유되는 광물종은 낮은 pH에서는 용해되어 불포화상태이나, pH가 중성으로 증가하면서 용해도가 낮아지면서 침전되어 높은 포화도를 보인다. 이로 인하여 본 연구지역 대상인 회산천 전역을 따라서 흰색 내지 회백색의 침전물이 다량 형성되는 것으로 판단된다.
대표적인 수산화철 광물종인 페리하이드라이트, 침철석(goethite)은 수계 전역에 걸쳐 높은 포화도를 보여 침전될 수 있음을 보여준다. 또한 적철석(hematite), 자로사이트(K-jarosite)도 일부 구간을 제외하면 높은 포화도를 나타낸다.
Table 3은 존재 가능한 화학종을 나타낸 것으로 황산이온은 대부분 SO42-의 이온상태가 가장 우세하며, 일부는 황산알루미늄 이온 AlSO4+로 존재한다. 다만 갱구 유출수인 BY-1에서는 일부 황산칼슘 이온 CaSO4(aq)으로 존재하는데, 순수 황산이온(SO42-)의 존재비율은 타 지점에 비하여 가장 낮다.
Table 3. Chemical species percentage in AMD waters calculated by Visual MINTEQ
철은 BY-1, BY-2에서만 일부가 3가철이온 상태로 존재하며, 대부분은 수산화철이온 상태로 존재한다. 특이하게도 BY-1에서만 철의 51%가 황산철이온인 FeSO4+로 존재한다.
알루미늄은 지표 산성수가 희석되거나 중화되어 pH 4.5~5 이상인 환경에서는 침전이 일어난다(Nordstrom and Ball, 1986). 본 연구수계에서 알루미늄은 타 이온에 비하여 훨씬 다양한 화학종으로 존재하는데, 대부분 Al(OH)4-, Al (OH)2+ AlOH2+, Al(OH)2+과 같은 수산화알루미늄이온과 황산알루미늄이온 AlSO4+, 그리고 일부는 순수 알루미늄이온(Al3+)으로 존재한다. 특히 독성이 강한 알루미늄이온은 회산천 상류부 비오염 지역과 최하류 단양천 합류직전 지점을 제외하면 회산천 계곡을 따라 널리 분포한다.
알루미늄 화학종들 가운데서 순수 알루미늄이온(Al3+)의 비율은 0.02~20.79%를 차지하며, 갱구 유출수의 영향을 강하게 받는 지점인 BY-1, BY-2과 백색 내지 회백색 침전물의 발달이 심한 지점들에서 상대적으로 높게 나타난다.
AMD 침전물의 광물종 분석: X-선 회절분석(XRD) 및 적외선 분광분석 결과
용해도는 용존이온의 농도와 pH, Eh 등과 같은 수질화학 환경에 따라서 변할 수 있으며, 결과적으로 광물종으로 표현되는 고상의 포화도, 불포화도가 결정된다. 그런데, 평형반응이 충분히 진행되지 않거나, 하천의 유속, 유량변화, 또는 일관성이 없는 농도변화가 수반될 경우 이론적인 포화지수는 실제 야외현장의 AMD내 침전물의 특성을 설명하는 데 한계가 있다. 이는 AMD가 실험실의 조건이 아니라 상시 변화하는 수계환경이므로 예측치와 실제 하상바닥에서 침전된 고상 간 차이가 발생하게 된다.
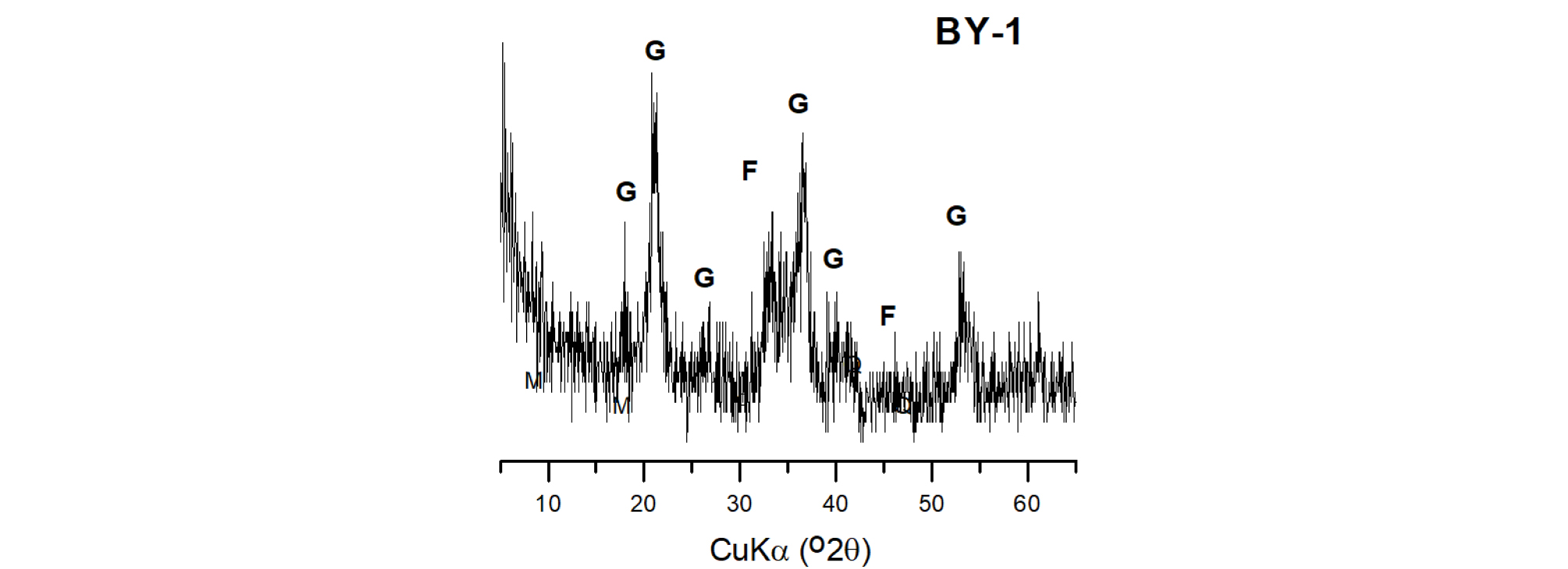
따라서 본 연구에서는 하상 내 침전물을 대상으로 이들의 광물종 분석을 수행하였다. 갱구 유출지점인 BY-1의 침전물은 Fig. 3에서 보는 것처럼 오렌지색을 띠는데, 이들을 대상으로 X-선 회절분석(XRD)을 실시하였다(Fig. 8). 이 침전물은 대부분 함철광물로서 주로 침철석, 페리하이드라이트와 같은 수산화철이 주를 이룬다. 회절선의 배경치가 높고 불균질한 특징으로 보아 비정질 광물종도 일부 포함되어 있는 것으로 파악된다.
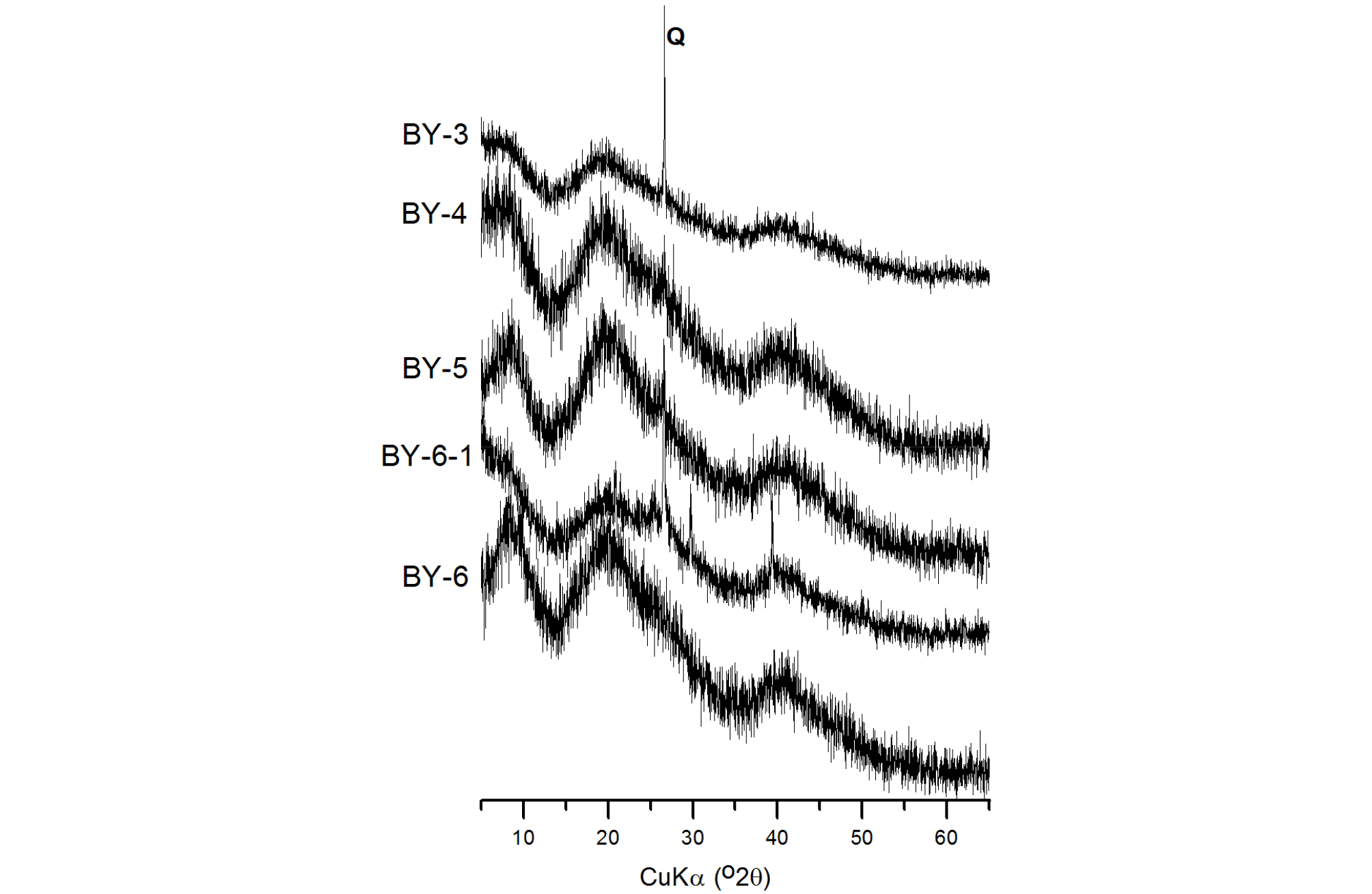
본 연구지역 주 하천인 회산천에 침전된 백색 내지 회백색 물질은 비정질의 특성이 매우 강한데, 이는 배스알루미나이트로 확인되었다(Fig. 9). BY-4, BY-5, BY-6에서 약간 결정도가 증가하지만, 전체적으로 배스알루미나이트의 결정도는 매우 낮다. 배스알루미나이트는 Table 2에서처럼 포화지수 계산상으로도 본 회산천 수계에서 과포화된 것으로 나타났는데, 실제 침전물의 광물종도 배스알루미나이트로 확인되었다. 그러나, 포화지수상 과포화 상태를 보인 여러 광물종, 특히 수산화알루미늄 광물은 배스알루미나이트 외에는 확인되지 않는다. 이는 수산화알루미늄 광물이 거의 비정질로 구성되기 때문에 XRD 분석상으로는 타 알루미늄광물의 존재가 파악되지 않기 때문이다. XRD 상으로 보면 결정도가 낮은 배스알루미나이트가 주를 이루나, 일부 회절선은 수산화알루미늄규소 광물종인 이모골라이트[imogolite, Al2SiO3(OH)4]와 비슷한 패턴을 보여준다. 그러나 주요 회절선의 위치와 결정격자의 층간간격(d-spacing)은 이모골라이트와는 잘 일치하지 않는다. 따라서 백색 내지 회백색의 침전물의 대부분은 결정도가 매우 낮은 배스알루미나이트인 것으로 감정된다.
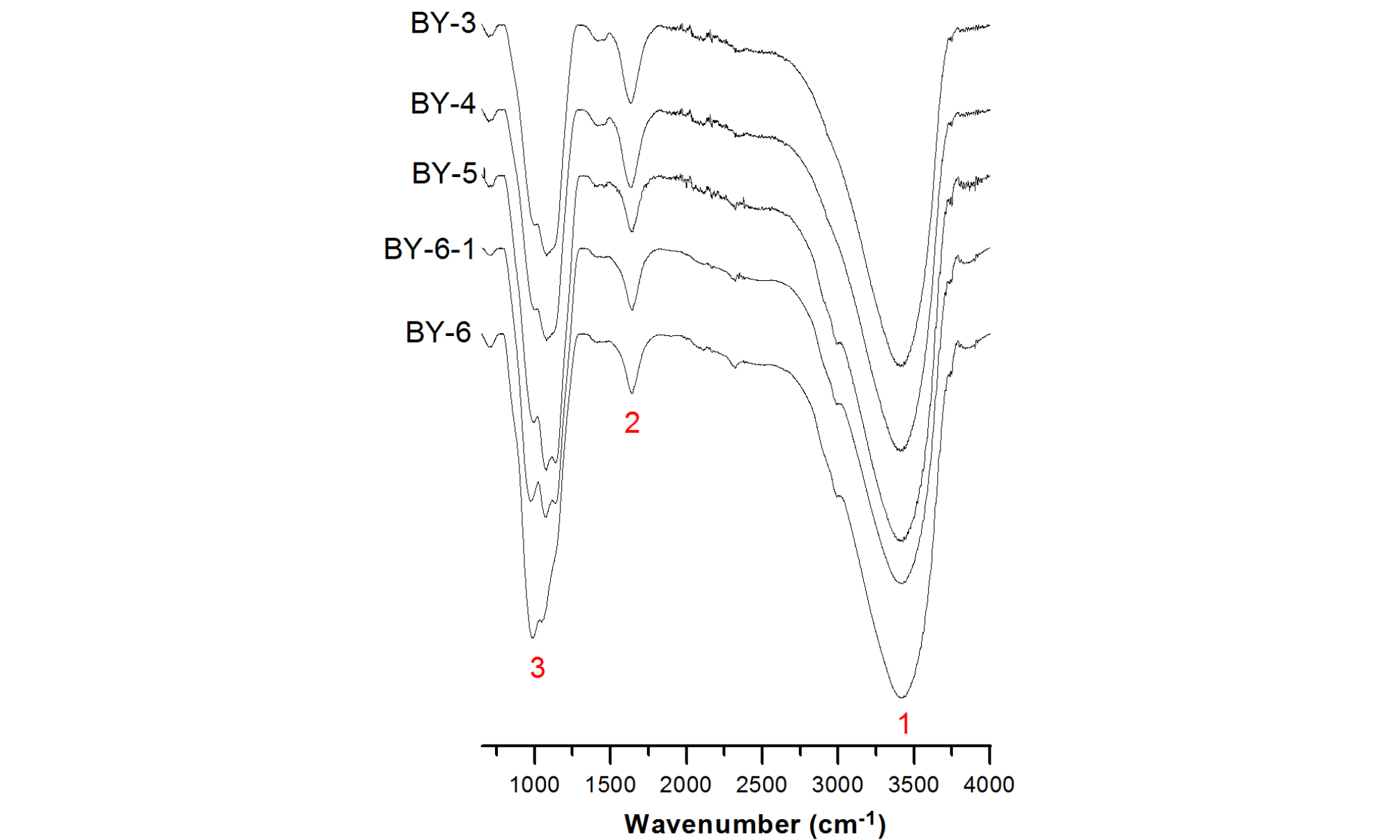
한편, 분자결합 특성 파악을 위하여 적외선분광분석 결과의 경우(Fig. 10), 파수 3400 cm-1 범위에서 큰 흡수선은 수산기의 신축진동(OH stretching vibration)이며, 1650 cm-1부근의 흡수선은 수산기의 굽힘진동(bending vibration)이며, 980~1100 cm-1 범위의 흡수선은 이중분리(doublet)를 보여 주는데, 이들은 황산이온(SO4)의 신축진동과 Al-O 신축진동에 해당한다. 이중분리선은 백색침전물이 다량 형성되는 지점의 시료(BY-6)에서 가장 약하게 나타난다. 이 같은 적외선분광 흡수선들은 배스알루미나이트의 특징과 잘 부합한다.
침전물의 초미세 구조적, 화학적 특징: 주사전자현미경 분석결과
흔히 AMD 내의 함철 침전물은 생화학적 반응의 결과물로 생성되며, 용존이온들의 용해도 변화에 따라서 고상으로 결정화된 산물로 간주할 수 있다. 따라서 침전물의 생성은 수계로부터 특정한 이온이 제거 또는 저감되는 과정이다. 그런데 AMD는 일반적인 수계에 비하여 매우 고농도로 이온이 용존되어 있을지라도, 지표상에서 반응이 일어나는 한계점 때문에 대부분의 경우 이러한 침전물은 결정도가 매우 낮거나, 마이크로미터 또는 나노미터 수준의 초미세 결정입자로 생성되는 경향이 있다. 따라서 침전물의 특성분석에 주사전자현미경(SEM)을 활용한 영상분석 및 화학분석은 매우 유용하다.
갱구유출수(BY-1)에서 흔히 발견되는 오렌지색의 침전물의 경우, 이들은 XRD 분석결과에 의하면 결정도가 낮은 철수산화물로 구성되어 있다. 이들 광물은 일부 비정질을 포함하지만 대부분 침철석과 페리하이드라이트이다. 이 시료를 주사전자현미경으로 관찰한 결과, 미세한 튜브형(tubular) 또는 배관처럼 보이는 칼집형(sheath)의 철박테리아의 군집체가 다량으로 함유되어 있음을 알 수 있다(Fig. 11). 이들은 철산화 박테리아의 일종인 Leptothrix orchracea인데, 내부와 표면에는 수십 나노미터 크기인 비정질의 나노 철수산화물이 구형의 집합체를 이루며 침착되어 있다. 특히 파괴된 단면에서는 이 같은 특징을 잘 관찰할 수 있다. 박테리아 튜브 내부에서도 나노미터 크기의 함철 결정들이 다량으로 부착되어 있는데, 이 같은 현상은 산성광산 배수 내에서 철의 침전작용 동안 화학적 반응 외에도 미생물학적 활동이 수반되어 있음을 보여준다. 특히 성게(urchin) 또는 밤송이 형태로 함철 결정의 집합체를 형성하는 슈베르트마나이트와 침철석이 이들 박테리아의 표면이나, 박테리아 개체 사이의 공간에서 흔히 생성되어 있는데, 이들은 성인적으로 서로 밀접한 관련성이 있는 것으로 보인다. 슈베르트마나이트는 수십 나노미터의 결정크기를 보여주며, 동일한 결정 내에서도 침철석으로 전이되는 중간형태도 일부 관찰된다.
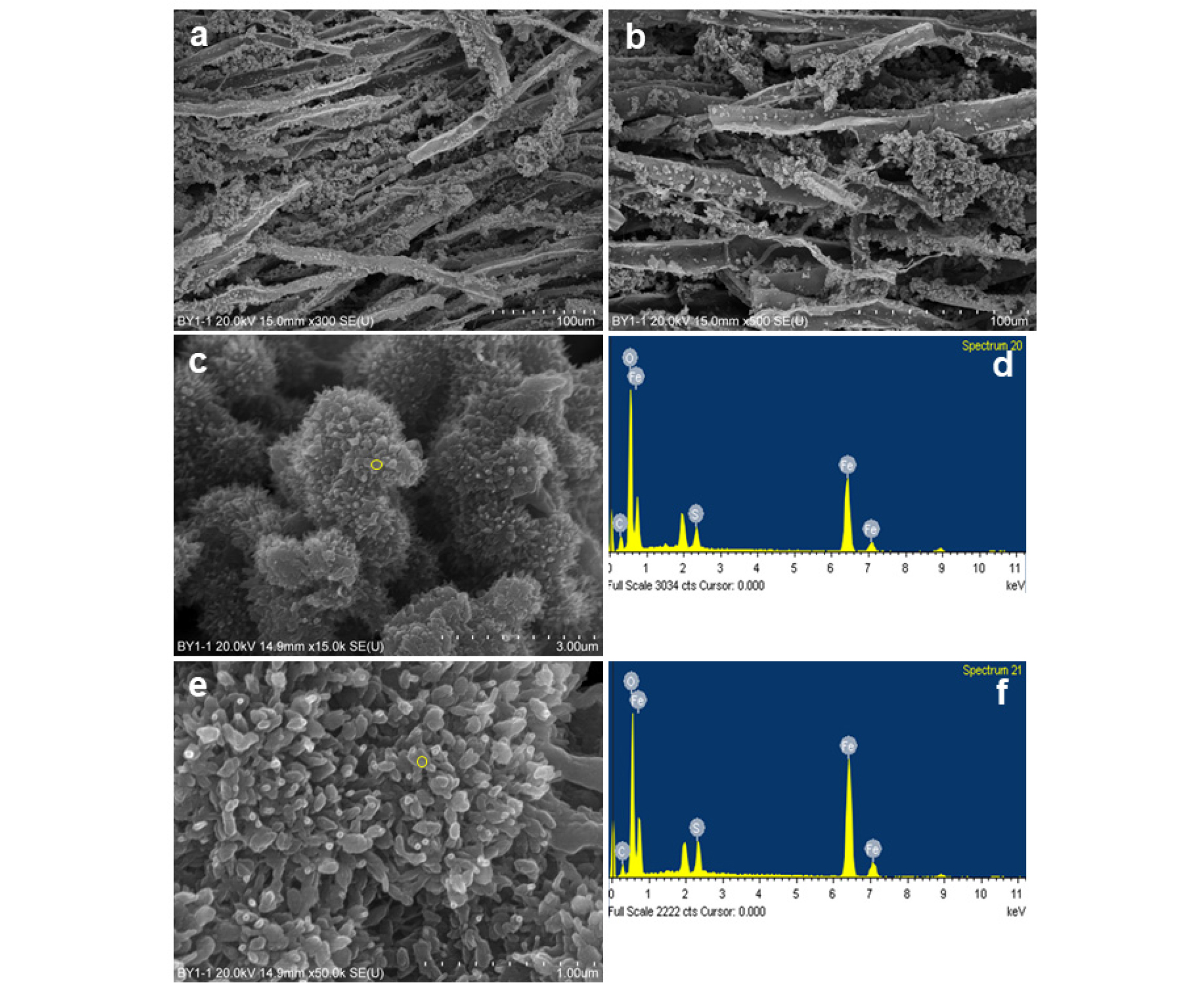
Fig. 11.
SEM micrographs of dark yellowish orange mass (BY-1) found in ochre deposition near pitmouth of Bongyang abandoned coal mine. (a) Aggregate of thin fibers or filamentous mass of Leptothrix ochracea. (b) Broken inner surface coating of iron oxyhydroxides with amorphous or irregular-shapes iron particles attached to the bacteria. (c) Urchin-like of aggregates showing abundant schwertmannite and lesser goethite. (d) EDS analysis on the yellow circle area of (c) showing chemical compositions of schwertmannite and goethite. (e) Urchin-like schwertmannite shows crystals with a few tens of nanometers in width. (f) EDS analysis on the yellow circle area of (e) showing schwertmannite and lesser goethite. Magnifications: (a) 300×, (b) 500×, (c) 15,000×, (e) 50,000×.
슈베르트마나이트는 달성광산, 동해광산, 태백탄전 등의 AMD 침전물에서도 확인된 바 있다(Yu et al., 1999; Choo and Lee, 2002; Kim et al., 2002, Kim et al., 2003; Choo et al., 2004, Choo et al., 2007, Choo et al., 2008). 에너지분광분석(EDS) 결과에 의하면, 이들 나노입자들은 산소와 철이 가장 풍부하며, 황, 탄소가 수반된다. 갱구유출수 지점의 오렌지색 침전물 시료인 BY-1은 철박테리아와 슈베르트마나이트가 풍부하며, 침철석이 일부 함유되어 있음을 보여준다.
AMD에서 박테리아와 관련된 수산화철 또는 수산화황산철의 생성은 다양한 작용에 의하여 일어나는데, 이차광물의 생성이나 수질변화는 화학적 반응 외에도 박테리아와 같은 미생물학적(microbial) 상호작용이 중요한 요소이다(Little et al., 1998; Banfield et al., 2000; Baker and Banfield, 2003; Johnson and Hallberg, 2003). 특히 산성환경 하에서 Thiobacillus ferroxidans는 철 수산화물이나 철황화수산화물의 침전을 촉진시킨다(Fortin et al., 1996; Chan et al., 2016). 중성 pH에서는 Leptothrix와 Gallionella에 의한 2가철의 산화작용은 약한 환원환경에서도 발생한다(Konhauser, 1997; Fleming et al., 2011). 본 시료의 경우, 일반적인 국내의 타 AMD(cf, Kim et al., 2002)에서 흔히 발견되는 Gallionella는 없으며, 그 대신에 Leptothrix가 생장하는 것이 특이하다.
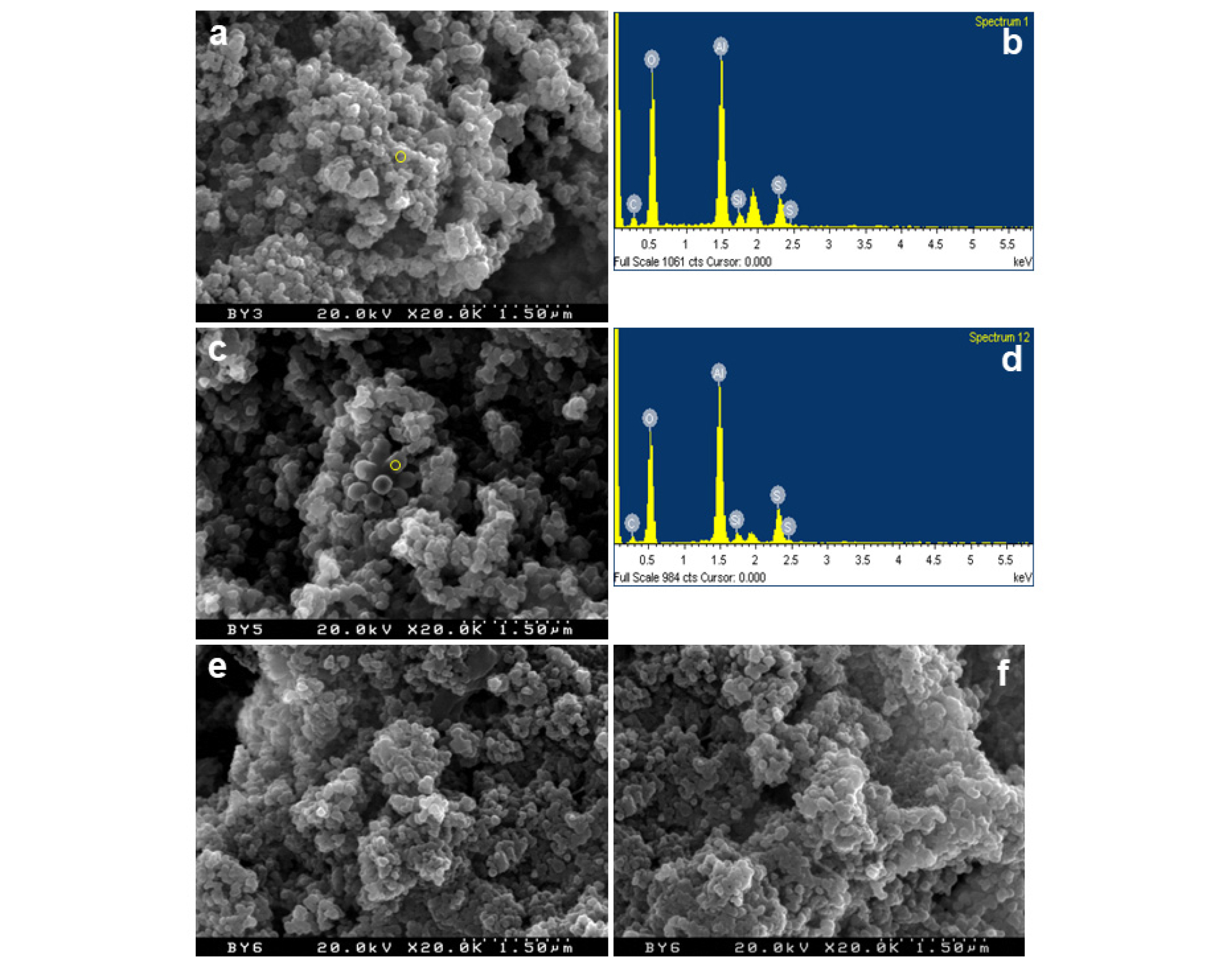
백색 내지 회백색의 침전물의 경우, 갱구입구 부근(BY-1지점)에서 발달하는 오렌지색 침전물과는 달리 상이한 미세특징을 보여준다. 예를 들면 수산화황산알루미늄 광물이 풍부한 BY-3, BY-5, BY-6의 경우 약간 납작한 타형의 비정질 입자특성을 나타낸다(Fig. 12). EDS 분석결과에 의하면 화학조성은 Al > O > S로 구성되어 있으며, Si, C는 소량으로 포함되어 있다. 본 침전물은 주로 배스알루미나이트로 구성되어 있음을 의미하는데, 이는 XRD 분석결과(Fig. 9)와도 잘 일치한다. 그러나 이들 시료에서는 철황박테리아와 같은 미생물의 존재는 확인되지 않는다. 이는 철, 황을 활용하는 박테리아가 생장할 수 있는 환경이 아니기 때문이다. 따라서 회산천 중하류 일대에서는 하상 침전물의 생성에 철황박테리아와 같은 미생물학적 기여는 없다고 판단된다. 백색 내지 회백색 침전물을 구성하고 있는 알루미늄질 광물의 결정도는 매우 낮으며, 결정입자의 직경은 대부분 100~200 nm로서 타형 내지 아원형을 이루는 것이 특징이다. 형태적인 특징으로 볼 때, 이런 함알루미늄 광물은 결정도가 매우 낮거나, 거의 비정질에 가까운 특성을 보인다.
배스알루미나이트질 침전물의 나노결정구조(nanocrystalline structure) 특징: 핵자기공명(27Al NMR)분석결과
27Al NMR은 결정구조에서 단거리 질서도(short-ordering)를 파악하는데 유용한데, 알루미늄의 배위수에 따라서 화학적 이동(chemical shift)는 다양하게 나타난다. 예들 들면 사면체 자리(tetrahedral site, AlIV)의 Al의 경우 50~90 ppm, 팔면체 자리(octahedral site, AlVI)의 Al은 0~15 ppm 범위, AlV는 30~41 ppm이다(Furrer et al., 2002; Kim et al., 2011; Carrero et al., 2017a, Carrero et al., 2017b). 따라서 알루미늄광물의 경우, 사면체자리의 Al과 팔면체자리의 Al을 구분하는데 매우 유용하다(Brown et al., 2003; Hiradate, 2004, Hiradate, 2005). 대부분의 알루미늄 수산화광물에서 팔면체자리의 Al은 -5~15 ppm 범위에서 나타나는 단일 신호가 크게 나타나며, 사면체자리의 Al은 50 ppm 이상에서 나타난다(Paris et al., 2007).
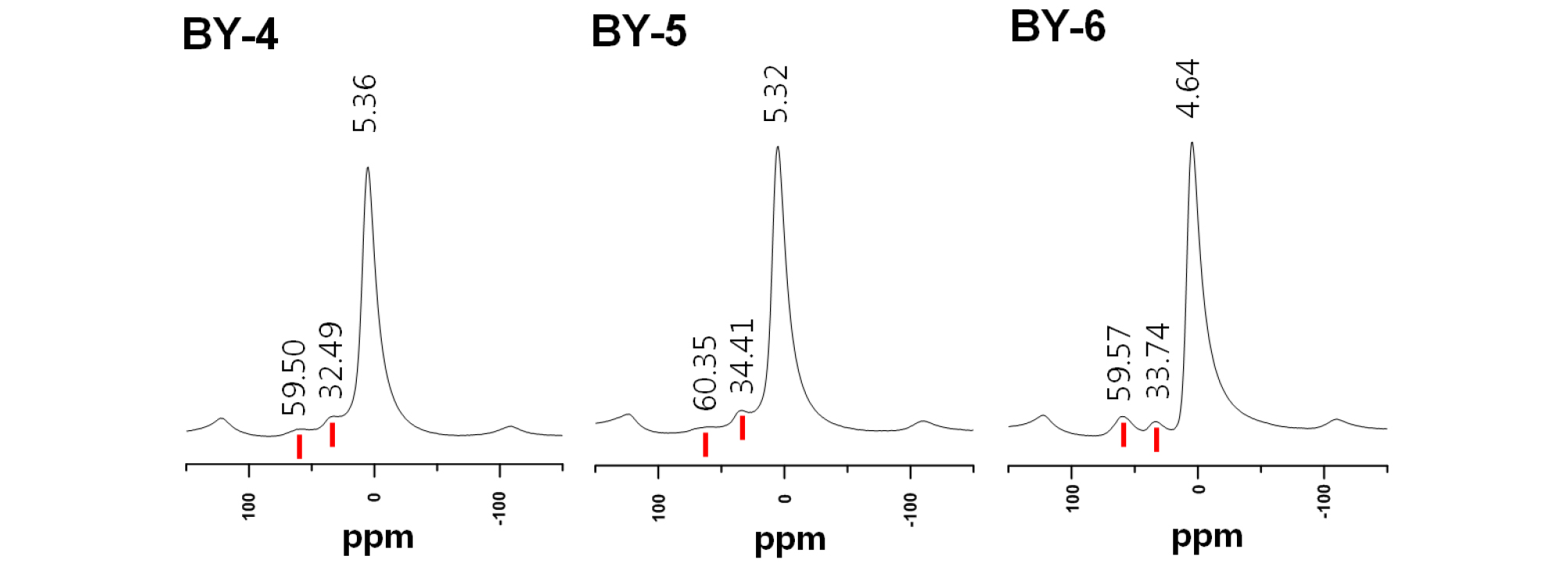
본 연구지역의 백색 내지 회백색 침전물의 생성이 뚜렷한 수계지점(BY-4, BY-5, BY-6)에서의 침전물의 27Al NMR은 다양한 화학적 이동값을 보이는데, 가장 강한 피크는 4.64~5.36 ppm에서 나타나며, 이는 팔면체자리의 Al에 해당된다(Fig. 13). 그 외에 32.49~33.74 ppm, 59.50~60.35 ppm 범위에서 약한 피크가 확인된다. 32.49~33.74 ppm 범위는 5배위 Al에 해당하며, 59.50~60.35 ppm 범위의 피크는 Al-중합체인 Al13-Tridecamer 에 해당된다. 이는 결정도가 매우 낮기 때문에 배스알루미나이트와 서로 혼재하는 것으로 보인다. 이 Al-중합체는 강원도 오십천 AMD에서도 산출이 확인된 바 있으며, 국내의 여러 폐탄광 AMD의 백색 침전물에서 형성될 가능성이 높다(Kim et al., 2011). 그러나 대부분의 경우, 국내 폐탄광 AMD 내 백색침전물에 대한 정밀한 분석이 수행되지 않아서, 여전히 이들 침전물의 구성물질 감정과 결정도 연구가 필요한 실정이다. 즉 이와 같은 침전물은 결정성이 매우 낮거나, 나노결정으로 생성되기 때문에 XRD나 일반적인 분석법으로는 감정이 어려우므로, 초고배율의 전자현미경이나 NMR과 같은 분광학적 연구가 요구된다.
알루미늄의 발생과 제어
용존 알루미늄은 독성이 강하므로 생태계와 인간환경에 매우 중요하다(Mortula et al., 2009). 용존 알루미늄 농도는 pH에 따라서 변하는데, 특히 폐석탄이나 탄질셰일 속에 함유되어 있는 운모류, 카올리나이트와 같은 알루미늄 규산염광물의 용해도와 2차생성물인 알루미늄 수산화물의 생성에 의해서 영향을 받을 수 있다(Bigham and Nordstrom, 2000).
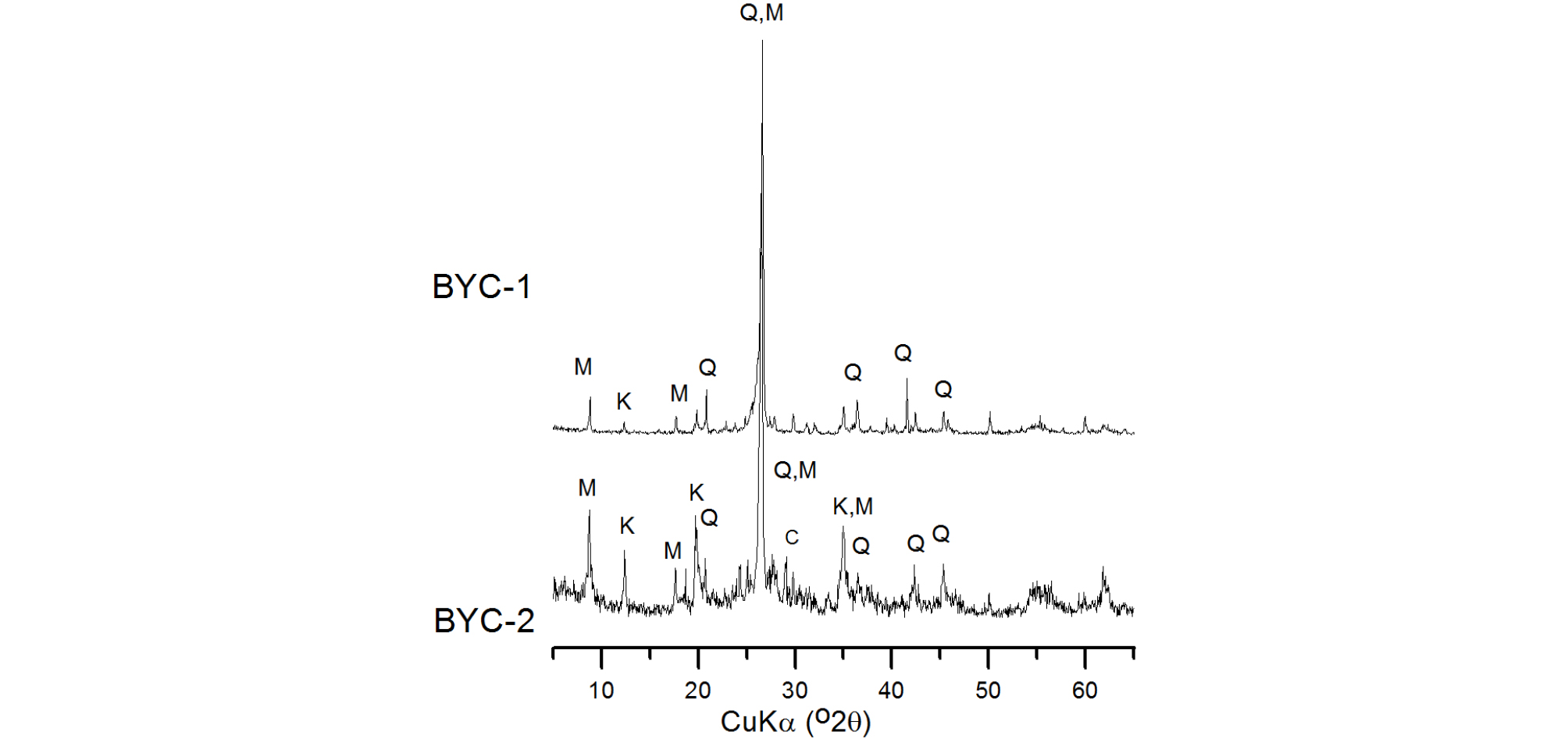
이곳 AMD 발생 근원암인 저품위 석탄폐석에 대한 XRD 분석결과에 의하면, 백운모, 카올리나이트, 석영 및 비정질의 탄(coal) 등으로 구성된다(Fig. 14). 황철석의 함량은 분석오차 미만으로 거의 확인되지 않는 수준이다. 폐탄에서는 고알루미늄 광물이 다량 함유되어 있으므로, 이들이 황철석의 산화작용으로 인해 산이 발생하고, 강산성 환경에서 알루미늄이 용해된 것으로 보인다. 봉양폐탄광은 이런 특성으로 인하여, AMD에 다량의 알루미늄이 용존된 것으로 해석된다.
수계 내의 알루미늄의 농도는 Figs. 5, 7에서 보듯이, 배스알루미나이트나 깁사이트와 같은 알루미늄 광물들의 침전에 의하여 급감한다. 즉 강산성 환경에서 용존되어 있던 알루미늄은 약산성, 중성 환경으로 가면서 결정화되어 침전하게 되면서 용존 알루미늄의 농도는 급감하게 된다. 이 같은 현상은 알루미늄의 용해도가 강산성에서 매우 높으나, 약산성~중성환경으로 가면서 급감하기 때문에 발생하는 지구화학적 특성에 기인한다.
본 연구지역에서 흔히 산출되는 배스알루미나이트는 나노결정질이 특징적인데, 이 광물은 대개 pH 4.5에서 고농도의 알루미늄과 황산이온 환경에서 잘 형성된다(Bigham and Nordstrom, 2000). 이는 Cu나 As같은 유해원소들과 친화력이 높아 결정의 표면에 공침이나 흡착되므로 환경적으로 매우 중요한 광물이다(Carrero et al., 2017a; Wanner et al., 2018).
따라서 봉양폐탄광 주변 및 회산천 일대에서는 AMD를 저감, 제어하기 위해서는 무엇보다 함알루미늄 광물의 침전과 용해를 조절하는 것이 중요하다. 특히 결정도가 매우 낮고, 나노결정질로 산출되는 수산화알루미늄, 수산화황산알루미늄 광물들은 화학적 반응성이 높고, 용해도는 조립질, 결정질에 비하여 높기 때문에 다소 불안정(metastable)하다. 결정도가 낮은 수산화광물은 많은 유해원소들을 흡착하기 때문에 환경적인 측면에서도 중요하다(Sánchez-España and Reyes, 2019). 따라서 AMD 수계의 환경, 특히 pH가 산성으로 변할 경우, 침전광물의 용해도가 변하므로 수계환경의 안정성도 변하게 된다. 즉 강산성 환경에서는 함 알루미늄 광물들은 쉽게 용해되기 때문에 결과적으로 AMD 수계에서 Al 독성 잠재력이 증가할 수 있으므로 이들의 제어가 필수적이다. 특히 배스알루미나이트, Al-중합체인 Al13-Tridecamer와 같은 결정도가 매우 낮은 광물들의 존재여부, 용해도와 침전특성에 관한 정보는 봉양폐탄광 AMD인 회산천 일대의 알루미늄의 거동특성을 제어하는 데 중요한 역할을 담당할 수 있다.
결 론
월악산 국립공원 상류에 위치하는 봉양폐탄광 AMD는 알루미늄을 다량 함유하고 있으며, 회산리 일대 하천바닥을 백색 침전물로 오염시키고 있다. 수질은 pH와 용존이온의 침전에 따라서 변화하며, 포화지수 계산결과 철, 알루미늄 광물종이 다수 과포화되어 있다. 오렌지색 침전물은 슈베르트마나이트와 침철석으로 구성되며, Leptothrix orchracea 박테리아가 생장한다. 하천의 합류로 인한 희석작용과 철황화물의 침전으로 인해 수계의 pH가 증가하는 회산천 본류지점에서는 백색 내지 회백색의 침전물이 다수 발달한다. 이들은 독성이 강한 알루미늄계열이 주를 이루는데, 가장 대표적인 광물종은 배스알루미나이트이며, 이것의 결정도는 매우 낮다. 이 백색질 알루미늄광물에서는 소량의 Al-중합체 Al13-Tridecamer가 포함되어 있는데, 배스알루미나이트의 매우 낮은 결정도와 성인적으로 밀접한 관련성이 있는 것으로 보인다. 봉양폐탄광 주변 및 회산천 일대에서의 AMD를 저감, 제어하기 위해서는 무엇보다 함알루미늄 광물의 침전과 용해도를 조절하는 것이 핵심인데, 지속적으로 중성환경을 유지할 필요가 있다.